استفاده منظم از مکملهای روغن ماهی و روند بیماریهای قلبی عروقی: مطالعه کوهورت آیندهنگر
مقدمه
بیماریهای قلبی عروقی به عنوان اصلیترین علت مرگ و میر در سراسر جهان شناخته میشوند و تقریباً یک ششم از کل مرگ و میرها در بریتانیا را به خود اختصاص میدهند. روغن ماهی، که منبع غنی از اسیدهای چرب امگا 3 شامل ایکوزاپنتانوئیک اسید و دوکوزاهگزانوئیک اسید است، به عنوان یک اقدام تغذیهای برای پیشگیری از این بیماریها توصیه شده است. مؤسسه ملی بهداشت و مراقبت بریتانیا به افرادی که در معرض خطر بالای بیماریهای قلبی عروقی هستند، توصیه میکند حداقل یک وعده ماهی چرب در هفته مصرف کنند. در سالهای اخیر، استفاده از مکملهای روغن ماهی در بریتانیا و سایر کشورهای غربی محبوبیت زیادی پیدا کرده است.
با اینکه برخی مطالعات اپیدمیولوژیک و بالینی اثرات اسیدهای چرب امگا 3 یا روغن ماهی بر بیماریهای قلبی عروقی و عوامل خطر آنها را بررسی کردهاند، نتایج به دست آمده متناقض بودهاند. آژانس تحقیقات و کیفیت مراقبتهای بهداشتی به طور سیستماتیک ۳۷ مطالعه مشاهدهای و ۶۱ کارآزمایی تصادفی کنترلشده را مرور کرده و شواهدی یافت که نشان میدهد مصرف بیشتر مکملهای روغن ماهی بر سکته ایسکمیک اثرات مفید دارد. با این حال، هیچ اثر مفیدی برای فیبریلاسیون دهلیزی، رویدادهای نامطلوب عمده قلبی عروقی، انفارکتوس میوکارد، سکته کلی یا مرگ ناشی از همه علل مشاهده نشد. در مقابل، مطالعه کاهش رویدادهای قلبی عروقی با استفاده از ایکوزاپنت اتیل (REDUCE-IT) نشان داد که این ماده میتواند خطر رویدادهای نامطلوب عمده قلبی عروقی را در بیماران با سطوح بالای تریگلیسرید کاهش دهد، بدون توجه به استفاده از استاتینها. با این حال، بیشتر این مطالعات تمایل داشتند که نقش روغن ماهی را در یک مرحله خاص از بیماری قلبی عروقی ارزیابی کنند. برای مثال، برخی مطالعات جمعیت مورد بررسی را به افرادی با یک بیماری قلبی عروقی خاص یا در معرض خطر بالای آن محدود کردند، در حالی که سایر مطالعات پایگاههای داده جمعیتهای عموماً سالم را بررسی کردهاند. این عوامل ممکن است مقایسه مستقیم اثرات اسیدهای چرب امگا 3 بر رویدادهای فیبریلاسیون دهلیزی یا تشدید بیشتر بیماری قلبی عروقی را محدود کنند. تعداد کمی از مطالعات به طور کامل نتایج خاص بیماریهای قلبی عروقی را مشخص کرده یا اثرات متفاوت بر اساس ویژگیهای پیچیده بیماری در شرکتکنندگان را مد نظر قرار دادهاند. بنابراین، در این مطالعه فرض کردیم که مکملهای روغن ماهی ممکن است اثرات مضر، مفید یا بیاثر بر رویدادهای مختلف بیماری قلبی عروقی در بیماران با شرایط بهداشتی مختلف داشته باشند.
بیشتر مطالعات قبلی در مورد ارتباط بین روغن ماهی و بیماریهای قلبی عروقی معمولاً بر یک نتیجه سلامت خاص تمرکز داشتند. همچنین، هیچ مطالعهای به دوره پیشرفت پویا بیماریهای قلبی عروقی، از وضعیت سالم (مرحله اولیه)، تا فیبریلاسیون دهلیزی (مرحله ثانویه)، رویدادهای نامطلوب عمده قلبی عروقی (مرحله ثالث) و مرگ (مرحله نهایی) نپرداخته است. روشن کردن این مسیر پیچیده در ارتباط با پیشرفت دقیق بیماریهای قلبی عروقی میتواند بینشهای مهمی برای پیشگیری یا درمان بیماری در مراحل بحرانی ارائه دهد. اینکه آیا روغن ماهی میتواند به طور متفاوت بر دوره پویا بیماری قلبی عروقی تأثیر بگذارد (یعنی از فیبریلاسیون دهلیزی به رویدادهای نامطلوب عمده قلبی عروقی، به نتایج خاص دیگر بیماریهای قلبی عروقی، یا حتی به مرگ) همچنان نامشخص است.
برای پر کردن این شکاف اطلاعاتی، مطالعهای گروهی طولی انجام دادیم تا ارتباط بین مکملهای روغن ماهی و نتایج بالینی خاص بیماریهای قلبی عروقی، از جمله فیبریلاسیون دهلیزی، رویدادهای نامطلوب عمده قلبی عروقی و مرگ ناشی از همه علل را در افراد بدون بیماری قلبی عروقی شناخته شده یا در معرض خطر بالای آن برای هدف پیشگیری اولیه، تخمین بزنیم. همچنین، اثرات تعدیلکننده مکملهای روغن ماهی بر روند بیماری، از فیبریلاسیون دهلیزی تا نتایج دیگر، را در افراد با بیماری قلبی عروقی شناخته شده برای هدف پیشگیری ثانویه ارزیابی کردیم.
روشها
بانک زیستی بریتانیا یک مطالعه گروهی مبتنی بر جامعه است که بیش از نیم میلیون نفر از ساکنان بریتانیا در سنین ۴۰ تا ۶۹ سال در زمان ثبتنام در آن شرکت کردهاند. شرکتکنندگانی که با NHS ثبتنام کردند و در شعاع ۳۵ کیلومتری یکی از ۲۲ مرکز ارزیابی بانک زیستی زندگی میکردند به این مطالعه دعوت شدند. بین ۱ مارس ۲۰۰۶ و ۳۱ ژوئیه ۲۰۱۰، یک بررسی پایه بر اساس پرسشنامه صفحه لمسی و مصاحبههای حضوری انجام شد تا ویژگیهای شخصی، اجتماعی-اقتصادی، سبک زندگی و اطلاعات مربوط به بیمارها جمعآوری شود.
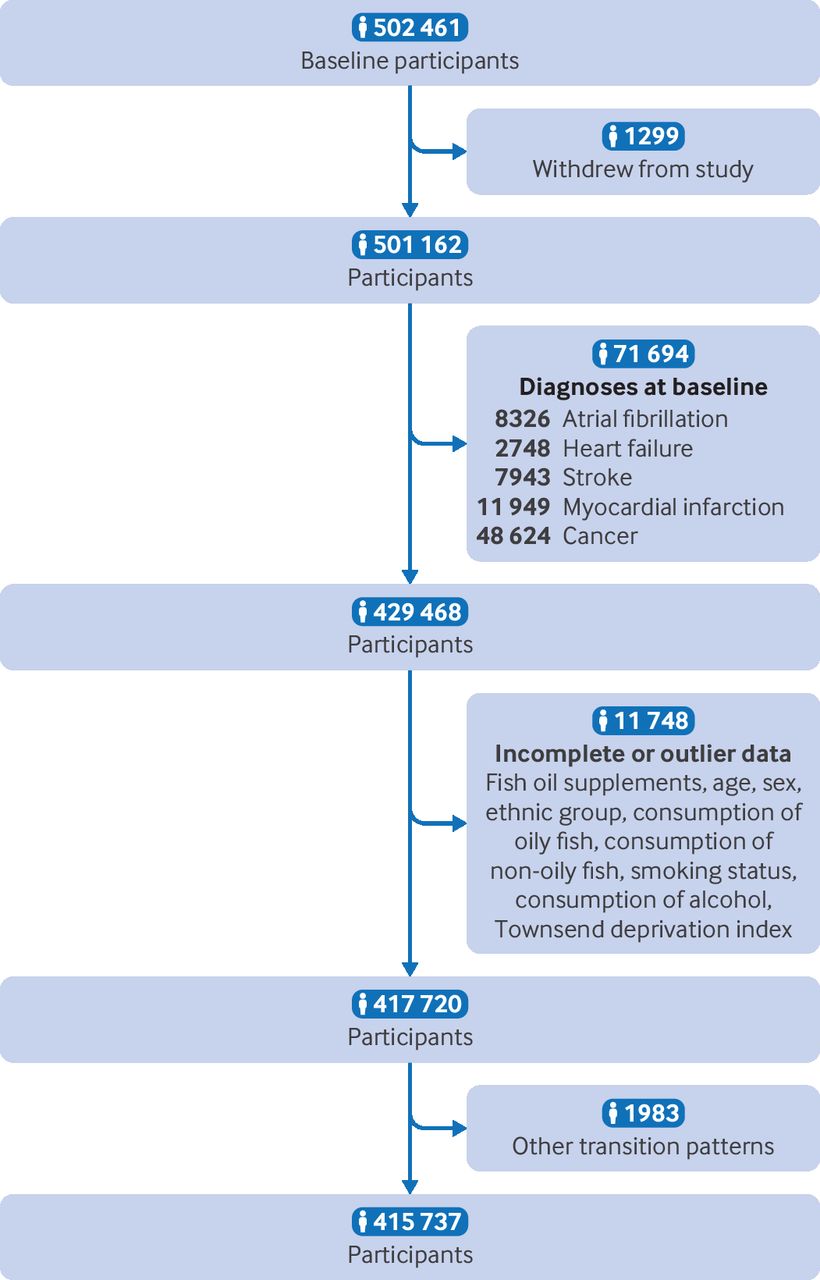
ما بیمارانی را که در زمان پایه تشخیص فیبریلاسیون دهلیزی (۸۳۲۶ نفر)، نارسایی قلبی (۲۷۴۸ نفر)، انفارکتوس میوکارد (۱۱۹۴۹ نفر)، سکته (۷۹۴۳ نفر) یا سرطان (۴۸۶۲۴ نفر) داشتند؛ کسانی که در طی پیگیری از مطالعه خارج شدند (۱۲۹۹ نفر)؛ یا کسانی که اطلاعات ناقص یا دور از انتظار برای اطلاعات اصلی داشتند (۱۱۷۴۸ نفر) را مستثنی کردیم. از آنجا که ما تنها بر یک دنباله خاص پیشرفت بیماری قلبی عروقی تمرکز کردیم (یعنی از وضعیت سالم به فیبریلاسیون دهلیزی، به رویدادهای نامطلوب عمده قلبی عروقی و سپس به مرگ)، ۱۹۸۳ شرکتکننده با الگوهای انتقال دیگر را مستثنی کردیم. ۴۱۵۷۳۷ شرکتکننده باقیمانده در این تحلیل گنجانده شدند.
تعیین استفاده از مکملهای روغن ماهی
اطلاعات مربوط به استفاده منظم از مکملهای روغن ماهی از طریق یک پرسشنامه لمسی خودگزارشدهی در طی بررسی پایه جمعآوری شد. از هر شرکتکننده پرسیده شد که آیا به طور منظم از هرگونه مکمل روغن ماهی استفاده میکند یا خیر. کارکنان آموزشدیده مصاحبهای شفاهی با شرکتکنندگان انجام دادند و از آنها پرسیدند که آیا در حال حاضر تحت درمان یا مصرف دارویی، از جمله مکملهای امگا ۳ یا روغن ماهی، هستند. بر اساس این اطلاعات، شرکتکنندگان به عنوان استفادهکنندگان منظم مکملهای روغن ماهی و غیر استفادهکنندگان طبقهبندی شدند.
پیگیری و نتایج
شرکتکنندگان از زمان ثبتنام تا زمان مرگ، یا تاریخ پایان مطالعه (۳۱ مارس ۲۰۲۱)، هر کدام که زودتر اتفاق بیفتد، مورد پیگیری قرار گرفتند. موارد جدید از جمله فیبریلاسیون دهلیزی، نارسایی قلبی، سکته و انفارکتوس میوکارد با ارتباط با ثبت مرگ، سوابق مراقبتهای اولیه و سوابق بستری در بیمارستان شناسایی شدند. اطلاعات مربوط به مرگها از ثبتهای مرگ NHS Information Centre برای شرکتکنندگان در انگلستان و ولز و از NHS Central Register Scotland برای شرکتکنندگان در اسکاتلند به دست آمد. نتایج با استفاده از کدهای سهکاراکتری ICD-10 (طبقهبندی بینالمللی بیماریها، ویرایش دهم) تعریف شدند. در این مطالعه، فیبریلاسیون دهلیزی با کد ICD-10 I48 و رویدادهای نامطلوب عمده قلبی عروقی با ترکیبی از کدهای نارسایی قلبی (I50، I11.0، I13.0 و I13.2)، سکته (I60-I64) و انفارکتوس میوکارد (I21، I22، I23، I24.1 و I25.2) تعیین شدند.
کووارییتها
ما دادههای پایه مربوط به سن (<۶۵ سال و ≥۶۵ سال)، جنسیت (مرد و زن)، گروه قومی (سفید و غیرسفید)، شاخص محرومیت تاونسند (با امتیاز بالاتر نشاندهنده سطوح بالاتر محرومیت)، وضعیت سیگار کشیدن (هرگز، سابق و فعلی) و مصرف الکل (هرگز، سابق و فعلی) را جمعآوری کردیم. دادههای مربوط به جنسیت از اطلاعات موجود در UK Biobank استخراج شده است و از جنسیتی که خود شرکتکنندگان گزارش کردهاند، استفاده نشده است. دادههای تغذیهای پایه از طریق پرسشنامه تغذیهای که توسط بیمار یا مصاحبهکننده تکمیل شده بود، جمعآوری شد. این پرسشنامه برای هر کشور (انگلستان، اسکاتلند و ولز) تنظیم شده بود تا مصرف معمول غذای فرد (ماهی چرب، ماهی غیرچرب، سبزیجات، میوه و گوشت قرمز) را ارزیابی کند. دیابت ملیتوس با استفاده از چندین روش مختلف در این مطالعه تعریف شد. ابتدا، از کدهای ICD-10 E10-E14 برای شناسایی بیماران دیابتی استفاده شد. همچنین، اگر بیماری توسط پزشک تشخیص داده شده و بیمار آن را گزارش کرده بود، به عنوان دیابت ثبت شد. علاوه بر این، اگر شرکتکنندگان اعلام کرده بودند که داروهای ضد دیابت مصرف میکنند، آنها نیز به عنوان دیابتی در نظر گرفته شدند. در نهایت، اگر سطح هموگلوبین A1c (که یک نشانگر مهم برای دیابت است) در زمان شروع مطالعه برابر یا بالاتر از ۶.۵٪ بود، آن فرد به عنوان دیابتی محسوب شد. فشار خون بالا در این مطالعه به چندین روش مختلف تشخیص داده شد. ابتدا، از کدهای ICD-10 I10 و I15 برای شناسایی بیماران مبتلا به فشار خون بالا استفاده شد. همچنین، اگر بیماری توسط پزشک تشخیص داده شده و بیمار این تشخیص را گزارش کرده بود، به عنوان فشار خون بالا ثبت شد. علاوه بر این، اگر شرکتکنندگان اعلام کرده بودند که داروهای ضد فشار خون مصرف میکنند، آنها نیز به عنوان دارای فشار خون بالا در نظر گرفته شدند. در نهایت، اگر فشار خون سیستولیک و دیاستولیک آنها در زمان شروع مطالعه برابر یا بیشتر از ۱۳۰/۸۵ میلیمتر جیوه بود، آن فرد نیز به عنوان مبتلا به فشار خون بالا محسوب شد. اطلاعات مربوط به سایر همبودیها (چاقی (ICD-10 E66)، بیماری مزمن انسدادی ریه (J44) و نارسایی مزمن کلیه (N18)) از اولین باری که این بیماریها در سوابق پزشکی افراد ثبت شده بودند، استخراج شدند. اطلاعات مربوط به استفاده از داروها، از جمله داروهای ضد فشار خون، داروهای ضد دیابت و استاتینها از سوابق درمان و استفاده از دارو استخراج شد. شاخصهای بیوشیمیایی بلافاصله پس از جمعآوری نمونههای سرم از شرکتکنندگان در زمان شروع مطالعه، در آزمایشگاه مرکزی اندازهگیری شدند. مصرف مفرط الکل به عنوان مصرف ≥۶ نوشیدنی استاندارد در روز برای زنان یا ≥۸ نوشیدنی استاندارد در روز برای مردان تعریف شد. اطلاعات دقیق مربوط به مصرف الکل و مصرف مفرط الکل در UK Biobank قبلاً گزارش شده بود.
تحلیل آماری
ویژگیهای شرکتکنندگان به دو صورت خلاصه شدند: برای متغیرهای دستهبندی شده، تعداد و درصد آنها محاسبه شد و برای متغیرهای پیوسته، میانگین و انحراف معیار (SD) ارائه شد. سپس، برای مقایسه ویژگیهای استفادهکنندگان منظم مکملهای روغن ماهی با غیر استفادهکنندگان، از آزمونهای آماری مختلفی استفاده شد. به طور خاص، از آزمون χ2 برای متغیرهای دستهبندی شده و از آزمون t دانشآموز برای متغیرهای پیوسته استفاده گردید.
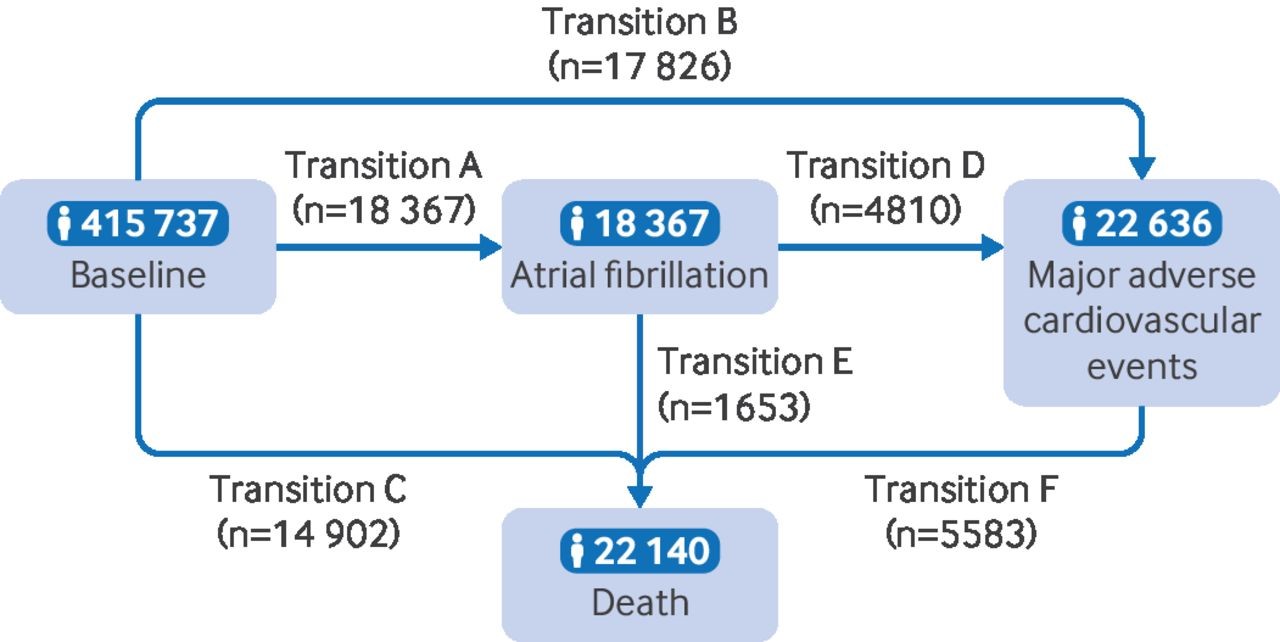
ما از یک مدل رگرسیون چند حالتی برای ارزیابی نقش استفاده منظم از مکملهای روغن ماهی در پیشرفت زمانی بیماری از وضعیت سالم به فیبریلاسیون دهلیزی، به رویدادهای نامطلوب عمده قلبی عروقی و در نهایت به مرگ استفاده کردیم. مدل چند حالتی یک توسعه از تحلیل بقا با ریسکهای رقابتی است. این مدل امکان تخمین همزمان نقش عوامل خطر در انتقال از وضعیت سالم به فیبریلاسیون دهلیزی (انتقال A)، وضعیت سالم به رویدادهای نامطلوب عمده قلبی عروقی (انتقال B)، وضعیت سالم به مرگ (انتقال C)، فیبریلاسیون دهلیزی به رویدادهای نامطلوب عمده قلبی عروقی (انتقال D)، فیبریلاسیون دهلیزی به مرگ (انتقال E) و رویدادهای نامطلوب عمده قلبی عروقی به مرگ (انتقال F) را فراهم میکند (الگوی انتقال I، شکل 2). تمرکز بر این شش انتقال به جای همه انتقالهای ممکن در وضعیت سلامت، از پیش برنامهریزی شده و مبتنی بر شواهد بود. اگر شرکتکنندگان در همان تاریخ وارد حالتهای مختلف شدند، از تاریخ حالت قبلی به عنوان تاریخ ورود به حالت بعدی منهای ۰.۵ روز استفاده کردیم.
ما تأثیرات استفاده منظم از مکملهای روغن ماهی را بر مسیرهای دیگر نیز بررسی کردیم. به عنوان مثال، ما رویدادهای نامطلوب عمده قلبی عروقی را به سه بیماری جداگانه (نارسایی قلبی، سکته و انفارکتوس میوکارد) تقسیم کردیم که منجر به سه مسیر مستقل شد (الگوهای انتقال II، III و IV، شکلهای مکمل آنلاین S1–S3). تمامی مدلها با توجه به سن، جنسیت، گروه قومی، شاخص محرومیت تاونسند، مصرف ماهی چرب، مصرف ماهی غیرچرب، وضعیت سیگار کشیدن، مصرف الکل، چاقی، فشار خون بالا، دیابت ملیتوس، بیماری مزمن انسدادی ریه، نارسایی مزمن کلیه و استفاده از استاتینها، داروهای ضد دیابت و داروهای ضد فشار خون تنظیم شدند.
موارد تکمیلی (جداول و نمودارهای اضافی و …)
تحلیلهای حساسیت
ما چندین تحلیل حساسیت برای الگوی انتقال A انجام دادیم. این تحلیلها شامل داده های اضافی برای مکان (شهری و روستایی)، شاخص توده بدنی (کموزن، نرمال، دارای اضافهوزن، و چاق)، و فعالیت بدنی (کم، متوسط و زیاد) بود. همچنین به جای مصرف الکل، مصرف مفرط الکل را در مدل قرار دادیم و متغیرهای دیگری از رژیم غذایی مانند مصرف سبزیجات، میوه و گوشت قرمز را نیز بررسی کردیم. ما زمان ورود شرکتکنندگان به وضعیتهای مختلف بیماری را بررسی کردیم و این کار را در فاصلههای زمانی مختلف انجام دادیم (مثلاً هر نیم سال، یک سال و دو سال). شرکتکنندگانی که در همان روز به چند وضعیت مختلف وارد شده بودند را حذف کردیم تا دادهها دقیقتر باشند. همچنین، رویدادهایی که در دو سال اول پیگیری رخ داده بودند را نادیده گرفتیم تا تأثیر آنها بر نتایج کاهش یابد. سپس تاریخ پیگیری را تا 31 مارس 2020 محدود کردیم تا تأثیر همهگیری کووید-19 را نیز در نظر بگیریم. از روش وزندهی احتمالی معکوس برای مقابله با انحرافات بین استفادهکنندگان منظم و غیر استفادهکنندگان مکملهای روغن ماهی استفاده کردیم. همچنین، تحلیلهای گروهی انجام دادیم تا ببینیم که آیا عوامل مختلفی مانند جنسیت، گروه سنی، گروه قومی، وضعیت سیگار کشیدن، مصرف ماهی چرب و غیرچرب، فشار خون بالا و استفاده از دارو بر نتایج تأثیر میگذارند یا ن.. تمامی تحلیلها با نرمافزار R و بسته mstate انجام شد و مقدار P دوطرفه کمتر از 0.05 به عنوان معنادار در نظر گرفته شد.
مشارکت بیماران و عموم
بیماران و عموم در طراحی، اجرا، گزارشدهی یا برنامههای انتشار این تحقیق دخیل نبودند. شرکتکنندگان در توسعه چارچوب اخلاق و حاکمیت برای بانک زیستی بریتانیا مشارکت داشتند و از طریق پرسشنامههای پیگیری و بازدیدهای ارزیابی اضافی در پیشرفت بانک زیستی بریتانیا درگیر بودند. بانک زیستی بریتانیا شرکتکنندگان را از تمامی نتایج تحقیق از طریق وبسایت مطالعه، رویدادهای شرکتکنندگان و خبرنامهها مطلع میکند.
نتایج
در مجموع 415,737 شرکتکننده با میانگین سنی 55.9 سال (انحراف معیار 8.1) و شامل 55% زنان در سنین 40-69 سال مورد تحلیل قرار گرفتند. از این تعداد، 31.4% (یعنی 130,365 نفر) در زمان شروع مطالعه گزارش دادند که به طور منظم از مکملهای روغن ماهی استفاده میکنند. جدول 1 ویژگیهای استفادهکنندگان منظم و غیر استفادهکنندگان مکملهای روغن ماهی را نشان میدهد. در گروه استفادهکنندگان منظم از مکملهای روغن ماهی، نسبت افراد مسن (22.6% در مقابل 13.9%)، افراد سفیدپوست (95.1% در مقابل 94.2%)، و زنان (57.6% در مقابل 53.9%) بیشتر بود. همچنین مصرف الکل (93.1% در مقابل 92.0%)، ماهی چرب (22.1% در مقابل 15.4%) و ماهی غیرچرب (18.0% در مقابل 15.4%) در این گروه بیشتر بود. شاخص محرومیت تاونسند و نسبت افراد سیگاری فعلی در استفادهکنندگان منظم از مکملهای روغن ماهی کمتر بود. جدول تکمیلی آنلاین S1 جزئیات بیشتری از ویژگیهای بیماران ارائه میدهد و جدول تکمیلی آنلاین S2 ویژگیهای پایه افراد شامل و مستثنیشده را مقایسه میکند.
در طول یک زمان میانگین مطالعه 11.9 سال، 18,367 شرکتکننده به فیبریلاسیون دهلیزی مبتلا شدند (انتقال A) و 17,826 شرکتکننده دچار رویدادهای نامطلوب عمده قلبی عروقی شدند (انتقال B)؛ 14,902 شرکتکننده بدون ابتلا به فیبریلاسیون دهلیزی یا رویدادهای نامطلوب عمده قلبی عروقی فوت کردند (انتقال C). در میان بیماران با فیبریلاسیون دهلیزی جدید، 4810 نفر به رویدادهای نامطلوب عمده قلبی عروقی مبتلا شدند (انتقال D) و 1653 نفر فوت کردند (انتقال E). در میان بیماران با رویدادهای نامطلوب عمده قلبی عروقی جدید، 5585 نفر در طول مطالعه فوت کردند (انتقال F، شکل 2). در تحلیلهای جداگانه برای بیماریهای فردی (الگوهای انتقال II، III و IV، شکلهای تکمیلی آنلاین S1–S3)، در بیماران با فیبریلاسیون دهلیزی، 3085 نفر به نارسایی قلبی، 1180 نفر به سکته و 1415 نفر به انفارکتوس میوکارد مبتلا شدند. در طول مطالعه، 2436، 2088 و 2098 مرگ در بیماران مبتلا به نارسایی قلبی، سکته و انفارکتوس میوکارد رخ داد.
ویژگیهای پایه شرکتکنندگان مطالعه بر اساس استفاده از مکملهای روغن ماهی
نتایج رگرسیون چند حالتی
جدول 2 نقشهای مختلف استفاده منظم از مکملهای روغن ماهی در انتقال از وضعیت سالم به فیبریلاسیون دهلیزی، به رویدادهای نامطلوب عمده قلبی عروقی و سپس به مرگ را نشان میدهد. برای افراد در مرحله اولیه (وضعیت سالم)، ما دریافتیم که استفاده از مکملهای روغن ماهی اثر مضری بر انتقال از وضعیت سالم به فیبریلاسیون دهلیزی دارد، با نسبت خطر تعدیل شده 1.13 (فاصله اطمینان 95%، 1.10 تا 1.17، انتقال A). نسبت خطر برای انتقال B (از وضعیت سالم به رویدادهای نامطلوب عمده قلبی عروقی) 1.00 (فاصله اطمینان 0.97 تا 1.04) و برای انتقال C (از وضعیت سالم به مرگ) 0.98 (0.95 تا 1.02) بود.
برای افراد در مرحله ثانویه (فیبریلاسیون دهلیزی) در آغاز مطالعه، استفاده منظم از مکملهای روغن ماهی خطر رویدادهای نامطلوب عمده قلبی عروقی را کاهش داد (انتقال D، نسبت خطر 0.92، فاصله اطمینان 95% 0.87 تا 0.98)، و اثر محافظتی مرزی بر انتقال از فیبریلاسیون دهلیزی به مرگ داشت (انتقال E، 0.91، 0.82 تا 1.01). برای انتقال F، از رویدادهای نامطلوب عمده قلبی عروقی به مرگ، پس از تعدیل برای کووارییتها، نسبت خطر 0.99 (0.94 تا 1.06، الگوی انتقال I، جدول 2) بود.
ما رویدادهای نامطلوب عمده قلبی عروقی را به سه بیماری جداگانه (یعنی نارسایی قلبی، سکته و انفارکتوس میوکارد) تقسیم کردیم و دریافتیم که استفاده منظم از مکملهای روغن ماهی با افزایش خطر سکته در افراد با وضعیت قلبی عروقی سالم همراه است (نسبت خطر 1.05، فاصله اطمینان 95%، 1.00 تا 1.11)، در حالی که اثر محافظتی در انتقال از وضعیت قلبی عروقی سالم به نارسایی قلبی مشاهده شد (نسبت خطر 0.92، فاصله اطمینان 95%، 0.86 تا 0.98). برای بیماران با فیبریلاسیون دهلیزی، ما دریافتیم که اثرات مفید استفاده منظم از مکملهای روغن ماهی برای انتقال از فیبریلاسیون دهلیزی به انفارکتوس میوکارد (نسبت خطر 0.85، فاصله اطمینان 95%، 0.76 تا 0.96)، و از فیبریلاسیون دهلیزی به مرگ (نسبت خطر 0.88، فاصله اطمینان 95%، 0.81 تا 0.95) وجود دارد (الگوی انتقال IV). برای بیماران با نارسایی قلبی، ما اثر محافظتی استفاده منظم از مکملهای روغن ماهی بر خطر مرگ را یافتیم (نسبت خطر 0.91، فاصله اطمینان 95%، 0.84 تا 0.99) (الگوهای انتقال II، III و IV، جدول 2).
تحلیلهای طبقهبندی شده و حساسیت
ما دریافتیم که سن، جنسیت، وضعیت سیگار کشیدن، مصرف ماهی غیرچرب، فشار خون بالا و استفاده از استاتینها و داروهای ضد فشار خون روابط بین استفاده منظم از مکملهای روغن ماهی و انتقال از وضعیتهای سالم به فیبریلاسیون دهلیزی را تعدیل میکنند (شکل تکمیلی آنلاین S4). ما دریافتیم که رابطه بین استفاده منظم از مکملهای روغن ماهی و خطر انتقال از وضعیتهای سالم به رویدادهای نامطلوب عمده قلبی عروقی در زنان (نسبت خطر 1.06، فاصله اطمینان 95%، 1.00 تا 1.11، ارزش P برای تعامل=0.005) و شرکتکنندگان غیرسیگاری (نسبت خطر 1.06، فاصله اطمینان 95%، 1.06 تا 1.11، ارزش P برای تعامل=0.001) بیشتر بود (شکل تکمیلی آنلاین S4). اثر محافظتی استفاده منظم از مکملهای روغن ماهی بر انتقال از وضعیتهای سالم به مرگ در مردان (نسبت خطر 0.93، فاصله اطمینان 95%، 0.89 تا 0.98، ارزش P برای تعامل=0.003) و شرکتکنندگان مسنتر (نسبت خطر 0.91، فاصله اطمینان 95%، 0.86 تا 0.96، ارزش P برای تعامل=0.002) بیشتر بود (شکلهای تکمیلی آنلاین S5 و S6). نتایج در تحلیلهای حساسیت به طور قابل توجهی تغییر نکردند (جدول تکمیلی آنلاین S3).
یافتههای اصلی
مطالعه ما استفاده منظم از مکملهای روغن ماهی را در روند پیشرفت بیماری قلبی عروقی، از وضعیت سالم (مرحله اولیه)، تا فیبریلاسیون دهلیزی (مرحله ثانویه)، رویدادهای نامطلوب عمده قلبی عروقی (مرحله ثالث) و مرگ (مرحله نهایی) بررسی کرد. در این تحلیل آیندهنگر از بیش از 400,000 بزرگسال بریتانیایی، ما دریافتیم که استفاده منظم از مکملهای روغن ماهی میتواند نقش متفاوتی در پیشرفت بیماری قلبی عروقی داشته باشد. برای افرادی با وضعیت قلبی عروقی سالم، استفاده منظم از مکملهای روغن ماهی، به عنوان یک گزینه پیشگیری اولیه، با افزایش خطر فیبریلاسیون دهلیزی همراه بود. با این حال، برای شرکتکنندگانی که تشخیص فیبریلاسیون دهلیزی داشتند، استفاده منظم از مکملهای روغن ماهی به عنوان پیشگیری ثانویه اثر محافظتی یا بیاثر بر انتقال از فیبریلاسیون دهلیزی به رویدادهای نامطلوب عمده قلبی عروقی، فیبریلاسیون دهلیزی به مرگ و رویدادهای نامطلوب عمده قلبی عروقی به مرگ داشت. هنگامی که رویدادهای نامطلوب عمده قلبی عروقی را به سه بیماری جداگانه (یعنی نارسایی قلبی، سکته و انفارکتوس میوکارد) تقسیم کردیم، روابطی یافتیم که نشاندهنده اثر خفیف مضر بین استفاده منظم از مکملهای روغن ماهی و انتقال از وضعیت قلبی عروقی سالم به سکته بود، در حالی که روابط مفید بالقوه بین استفاده منظم از مکملهای روغن ماهی و انتقال از فیبریلاسیون دهلیزی به انفارکتوس میوکارد، فیبریلاسیون دهلیزی به مرگ و نارسایی قلبی به مرگ مشاهده شد.
مقایسه با مطالعات دیگر
پیشگیری اولیه
مزایای قلبی عروقی استفاده منظم از مکملهای روغن ماهی در بسیاری از مطالعات بررسی شده است، اما نتایج متناقض هستند. با گسترش گزارشهای قبلی، مطالعه ما ارتباطات بین استفاده منظم از مکملهای روغن ماهی و نتایج خاص بیماری قلبی عروقی بالینی در افرادی بدون بیماری قلبی عروقی شناختهشده را تخمین زد. یافتههای ما با نتایج چندین کارآزمایی تصادفی کنترلشده و متاآنالیزهای قبلی مطابقت دارد. به عنوان مثال، مطالعه STRENGTH گزارش کرد که مصرف ۴ گرم در روز از اسیدهای چرب امگا ۳ دریایی با خطر ۶۹ درصد بالاتر فیبریلاسیون دهلیزی جدید در افراد با خطر بالای بیماری قلبی عروقی همراه بود. یک متاآنالیز از هفت کارآزمایی تصادفی کنترلشده نشان داد که مصرفکنندگان مکملهای اسیدهای چرب امگا ۳ دریایی خطر بیشتری برای وقوع رویدادهای فیبریلاسیون دهلیزی داشتند، با نسبت خطر 1.25 (فاصله اطمینان 95%، 1.07 تا 1.46، P=0.013). با این حال، مطالعه ریتم ویتامین D و امگا-۳ (VITAL Rhythm study)، یک کارآزمایی بزرگ برای پیشگیری اولیه از بیماری قلبی عروقی در بزرگسالان ۵۰ سال و بالاتر، هیچ اثری بر وقوع فیبریلاسیون دهلیزی جدید، رویدادهای نامطلوب عمده قلبی عروقی یا مرگ ناشی از بیماری قلبی عروقی در میان کسانی که با 840 میلیگرم در روز اسیدهای چرب امگا ۳ دریایی درمان شده بودند، در مقایسه با دارونما، نیافت.
یکی از توضیحات ممکن برای نتایج ناهماهنگ در این مطالعات این است که اثرات مضر ممکن است به دوز و ترکیب وابسته باشد. دوزهای بالاتر اسیدهای چرب امگا ۳ که در مطالعات قبلی استفاده شدهاند ممکن است نقش مهمی در ایجاد اثر مضر بر فیبریلاسیون دهلیزی داشته باشند. یک مطالعه نشان داد که غلظتهای بالای روغن ماهی خواص غشای سلولی را تغییر داده و فعالیت پمپ Na-K-ATPase را مهار میکند، در حالی که غلظت پایین روغن ماهی پتانسیل پراکسیداسیون را به حداقل رسانده و فعالیت را بهینه میکند. در مطالعه دیگری، افراد با فیبریلاسیون دهلیزی یا فلوتر درصدهای بالاتری از اسیدهای چرب غیراشباع چندگانه کل، و اسیدهای چرب غیراشباع n-3 و n-6، در غشاهای سلولهای قرمز خون نسبت به کنترلهای سالم داشتند.
در مورد ترکیب اسیدهای چرب امگا ۳، یک متاآنالیز اخیر نشان داد که ایکوزاپنتانوئیک اسید به تنهایی میتواند مؤثرتر از ترکیب ایکوزاپنتانوئیک اسید و دوکوزاهگزانوئیک اسید در کاهش خطر بیماری قلبی عروقی باشد. نتایج مشابهی در مطالعه INSPIRE گزارش شد که نشان داد سطوح بالاتر دوکوزاهگزانوئیک اسید مزایای قلبی عروقی ایکوزاپنتانوئیک اسید را هنگام تجویز بهصورت ترکیبی کاهش میدهد. توضیح دیگری ممکن است این باشد که سن، جنسیت، گروه قومی، وضعیت سیگار کشیدن، الگوهای غذایی و استفاده از استاتینها و داروهای ضد دیابت توسط شرکتکنندگان ممکن است اثرات استفاده منظم از مکملهای روغن ماهی بر رویدادهای بیماری قلبی عروقی را تعدیل کنند. با وجود این تفاوتها در تخمینهای خطر، یافتههای ما از استفاده از مکملهای روغن ماهی یا اسیدهای چرب امگا ۳ برای پیشگیری اولیه از فیبریلاسیون دهلیزی جدید یا دیگر رویدادهای خاص بیماری قلبی عروقی بالینی در افراد عموماً سالم حمایت نمیکنند. احتیاط در استفاده از مکملهای روغن ماهی برای پیشگیری اولیه به دلیل مزایای قلبی عروقی نامشخص ممکن است لازم باشد.
پیشگیری ثانویه
مطالعه بزرگ مقیاس ما نقش استفاده منظم از مکملهای روغن ماهی را در فرآیند بیماری، از فیبریلاسیون دهلیزی به مراحل جدیتر بیماری قلبی عروقی و تا مرگ، در افراد با بیماری قلبی عروقی شناختهشده ارزیابی کرد. برخلاف مشاهدات برای پیشگیری اولیه، ما ارتباطاتی یافتیم که میتواند نشاندهنده اثرات مفید بین استفاده منظم از مکملهای روغن ماهی و بیشتر انتقالهای بیماری قلبی عروقی باشد. هیچ ارتباطی بین استفاده منظم از مکملهای روغن ماهی و انتقال از فیبریلاسیون دهلیزی به مرگ یا از رویدادهای نامطلوب عمده قلبی عروقی به مرگ یافت نشد.
مطابق با فرضیه ما، مطالعه Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto Miocardico (GISSI) Prevenzione گزارش کرد که تجویز نسخههای با دوز کم از اسیدهای چرب غیراشباع چندگانه n-3 با کاهش رویدادهای قلبی عروقی در بیماران با انفارکتوس میوکارد اخیر مرتبط است. یک متاآنالیز از 16 کارآزمایی تصادفی کنترلشده نیز تمایل به اثرات مفید بیشتر برای پیشگیری ثانویه در بیماران با بیماری قلبی عروقی را گزارش کرد. چرا بیماران با فیبریلاسیون دهلیزی قبلی از مزایا بهرهمند میشوند، مشخص نیست. این یافتهها نشان میدهند که اثرات مستقل از تریگلیسریدهای اسیدهای چرب امگا ۳ ممکن است بهطور جزئی مسئول مزایای بیماری قلبی عروقی مشاهدهشده در کارآزماییهای قبلی باشند. با این حال، هیچ مکانیسم بیولوژیکی اثباتشدهای برای این توضیح وجود ندارد و دوز و فرمولاسیون اسیدهای چرب امگا ۳ که در عمل بالینی استفاده میشوند، شناختهشده نیستند.
برای فرآیند بیماری، از بیماری قلبی عروقی تا مرگ، یافتههای ما با نتایج کارآزماییهای پیشگیری ثانویه از اسیدهای چرب امگا ۳ که عمدتاً نشاندهنده اثرات پیشگیرانه ضعیف یا خنثی بر مرگ ناشی از همه علل با مکملهای روغن ماهی هستند، سازگار است. کارآزمایی نارسایی قلبی GISSI (GISSI-HF)، که در 6975 بیمار با نارسایی قلبی مزمن انجام شد، گزارش کرد که مکملهای اسیدهای چرب امگا ۳ خطر مرگ ناشی از همه علل را به میزان 9% کاهش دادند (نسبت خطر 0.91، فاصله اطمینان 95% 0.833 تا 0.998، P=0.041). Zelniker و همکاران نشان دادند که اسیدهای چرب امگا ۳ با کاهش شیوع مرگ ناگهانی قلبی در بیماران با سندرم حاد کرونری بدون ارتقای قطعه ST مرتبط هستند. یک متاآنالیز دریافت که استفاده از مکملهای امگا ۳ به میزان ≤1 کپسول در روز با مرگ ناشی از همه علل مرتبط نیست، اما در میان شرکتکنندگانی با خطر بیماری قلبی عروقی، مصرف دوز بالاتر با کاهش مرگ قلبی و مرگ ناگهانی مرتبط است. افرادی که ممکن است بیشترین بهره را از مکملهای روغن ماهی یا اسیدهای چرب امگا ۳ ببرند، احتمالاً افرادی آسیبپذیرتر، مانند کسانی با بیماریهای قلبی عروقی قبلی و کسانی که دیگر قادر به زندگی در جامعه نیستند، هستند. چگونگی توقف مکملهای روغن ماهی از بدتر شدن بیشتر بیماری قلبی عروقی مشخص نیست، اما نظریهای وجود دارد که مکملهای اسیدهای چرب امگا ۳ ممکن است از شریان کرونری محافظت کنند، که نشان میدهد اسیدهای چرب امگا ۳ دارای اثرات ضد التهابی و ضد هیپرتریگلیسریدمی هستند، که به کاهش ترومبوز و بهبود عملکرد اندوتلیال کمک میکنند. با این حال، اثرات اسیدهای چرب امگا ۳ بسته به استفاده قبلی فرد از استاتینها، میتواند متفاوت باشد، که ممکن است تا حدی توضیحدهنده اثرات متفاوت مکملهای روغن ماهی در افراد با و بدون بیماری قلبی عروقی باشد.
بسیاری از مطالعات اسیدهای چرب امگا ۳، از جمله کارآزماییهای بالینی بزرگ مقیاس و متاآنالیزها، نتایج کاملاً سازگاری ارائه نکردهاند. مطالعه ما عمدتاً اثرات بالقوه متفاوت استفاده منظم از مکملهای روغن ماهی بر پیشرفت بیماری قلبی عروقی را بررسی کرد و یک دید اولیه از این بحث مستمر ارائه داد. یافتههای ما پیشنهاد میکنند که احتیاط در استفاده از مکملهای روغن ماهی برای پیشگیری اولیه به دلیل مزایای قلبی عروقی نامشخص و اثرات مضر ممکن است لازم باشد. مطالعات بیشتری برای تعیین این که آیا عوامل مخدوشکننده بالقوه اثرات مکملهای روغن ماهی را تعدیل میکنند و مکانیزمهای دقیق مربوط به توسعه و پیشآگهی رویدادهای بیماری قلبی عروقی نیاز است.
نقاط قوت و محدودیتهای این مطالعه
نقاط قوت مطالعه ما شامل اندازه بزرگ نمونه، دوره پیگیری طولانی که به ما امکان تحلیل بیماریهای جدید تشخیص داده شده بالینی را داد، و دادههای کامل بر روی نتایج بهداشتی بود. استراتژی تحلیلی ما نیز یک نقطه قوت بود. مدل چند حالتی تخمینهای کمتر مغرضانهای نسبت به مدل کوکس مرسوم ارائه میدهد و اثر استفاده منظم از مکملهای روغن ماهی بر هر انتقال در مسیر بیماری قلبی عروقی را تفکیک میکند.
مطالعه ما دارای برخی محدودیتها نیز بود. اولاً، به عنوان یک مطالعه مشاهدهای، هیچ رابطه علی نمیتوان از یافتههای ما برداشت کرد. ثانیاً، اگرچه ما برای چندین کووارییت تنظیم کردیم، همچنان ممکن است مخدوشگرهای باقیمانده وجود داشته باشد. ثالثاً، اطلاعاتی درباره دوز و فرمولاسیون مکملهای روغن ماهی در این مطالعه در دسترس نبود، بنابراین نمیتوانستیم اثرات وابسته به دوز را ارزیابی کرده یا بین اثرات فرمولاسیونهای مختلف روغن ماهی تمایز قائل شویم. چهارم، استفاده از دادههای بستری بیمارستان برای تعیین رویدادهای فیبریلاسیون دهلیزی ممکن است برخی از رویدادهای تحریکشده توسط اپیزودهای حاد مانند جراحی، تروما و شرایط مشابه را حذف کرده باشد، که منجر به کاهش تخمین واقعی خطر میشود زیرا فیبریلاسیون دهلیزی تشخیص داده نشده یک وقوع رایج است. پنجم، بیشتر شرکتکنندگان در این مطالعه از گروه قومی سفیدپوست بودند و مشخص نیست که آیا یافتهها قابل تعمیم به گروههای قومی دیگر هستند یا خیر. نهایتاً، مطالعه ما تغییرات رفتاری در جمعیتهای با پروفایلهای قلبی عروقی مختلف را به دلیل اطلاعات محدود در نظر نگرفت و تغییرات در نتایج برای وضعیتهای مختلف قلبی عروقی نیاز به بررسی بیشتر دارد.
نتیجهگیری
این مطالعه آیندهنگر بزرگ از یک گروه بریتانیایی پیشنهاد میکند که استفاده منظم از مکملهای روغن ماهی ممکن است نقشهای متفاوتی در مسیر بیماری قلبی عروقی داشته باشد. استفاده منظم از مکملهای روغن ماهی ممکن است یک عامل خطر برای فیبریلاسیون دهلیزی و سکته در میان جمعیت عمومی باشد، اما میتواند برای پیشرفت بیماری از فیبریلاسیون دهلیزی به رویدادهای نامطلوب عمده قلبی عروقی و از فیبریلاسیون دهلیزی به مرگ مفید باشد. مطالعات بیشتری برای تعیین اینکه آیا عوامل مخدوشکننده بالقوه اثرات مکملهای روغن ماهی را تعدیل میکنند و مکانیزمهای دقیق مربوط به توسعه و پیشآگهی رویدادهای بیماری قلبی عروقی لازم است.